

ニューロライト®第一
このコンテンツは医療従事者向けの内容です。
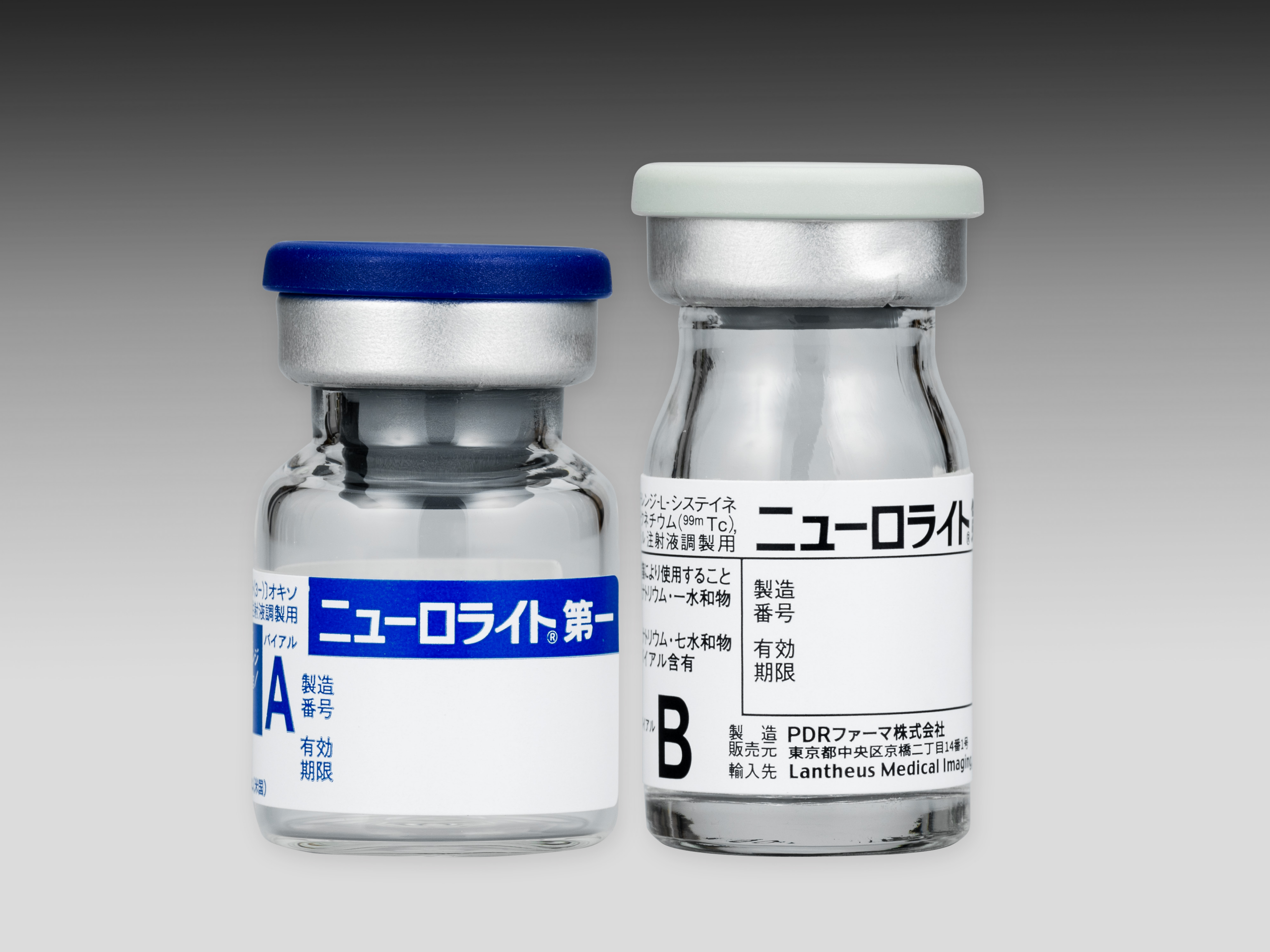
ニューロライト®第一
・用時調製が可能です。
放射性医薬品基準
[N,N’-エチレンジ-L-システイネート(3-)]オキソテクネチウム(99mTc)、ジエチルエステル注射液調製用
効能・効果
4. 効能又は効果
局所脳血流シンチグラフィ
用法・用量
6. 用法及び用量
〈[N,N’-エチレンジ-L-システイネート(3-)]オキソテクネチウム(99mTc),ジエチルエステル注射液の調製〉
・放薬基「過テクネチウム酸ナトリウム(99mTc)注射液ジェネレータ」の溶出液400~800MBq(3mL以下)をバイアルBに加える。
・日局生理食塩液3.0mLをバイアルAに加えて振り混ぜ、内容物を溶かす。
・バイアルAの溶液1.0mLを直ちにバイアルBに加えて振り混ぜ、室温に30分間静置する。
〈局所脳血流シンチグラフィ〉
通常、成人には400~800MBqを静脈内に投与し、投与5分以降より被検部にガンマカメラ等の検出部を向け撮像もしくはデータを収録し、脳血流シンチグラムを得る。
なお、投与量は、年齢、体重および検査方法により適宜増減する。
組成
本品は、バイアルA及びバイアルBの2バイアルにて構成される。
| 販売名 | ニューロライト®第一 | |
|---|---|---|
| バイアルA | バイアルB | |
| 有効成分 | 1バイアル中 N,N’-(1,2-エチレン)ビス-L-システインジエチルエステル二塩酸塩 0.90mg |
― |
| 添加剤 | 1バイアル中 塩化スズ(Ⅱ)二水和物 0.072mg、エデト酸ナトリウム水和物 0.36mg、D-マンニトール 24.0mg、塩酸 適量 |
1バイアル中 1mL リン酸二水素ナトリウム一水和物 0.460mg、リン酸水素二ナトリウム七水和物 4.105mg |
* 詳細は添付文書をご参照ください。
基本情報
-
販売名
ニューロライト®第一
-
承認年月日
1994年1月19日
-
承認番号
20600AMY00006000
-
再審査結果公表年月
2004年3月
-
薬価基準収載医薬品コード
4300443 G 1022
-
包装単位
2セット[1セット(Aバイアル、Bバイアル)×2]、5セット[1セット(Aバイアル、Bバイアル)×5]
サポート情報
製品のお問い合わせは、PDRファーマ株式会社で承っております。電話またはWeb(お問い合わせフォーム)より、お問い合わせください。
PDRファーマ株式会社
製品情報センター
受付時間9:00~17:00(土曜・日曜・祝日・当社休業日を除く)
*フリーダイヤルをご利用いただけない場合は、
03-3538-3624へお掛け直しください。
※内容を正確に確認するために通話を録音させて頂いております。あらかじめご了承ください。
関連製品
-
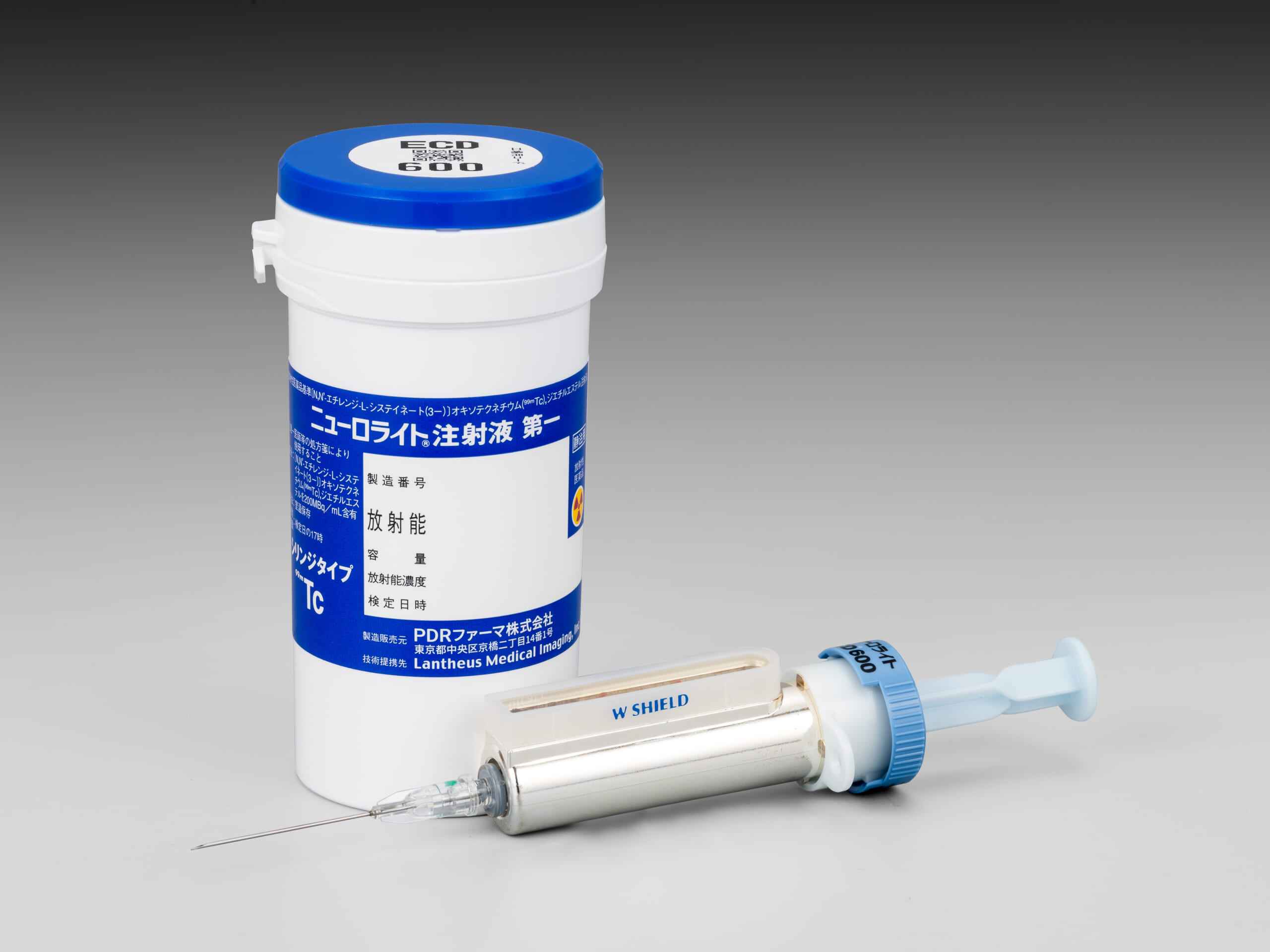 ニューロライト®注射液第一局所脳血流診断薬
ニューロライト®注射液第一局所脳血流診断薬
[N,N’-エチレンジ-L-システイネート(3-)]オキソテクネチウム(99mTc),ジエチルエステル注射液 -
 ニューロライト®第一局所脳血流診断薬
ニューロライト®第一局所脳血流診断薬
[N,N’-エチレンジ-L-システイネート(3-)]オキソテクネチウム(99mTc),ジエチルエステル注射液 調製用 -
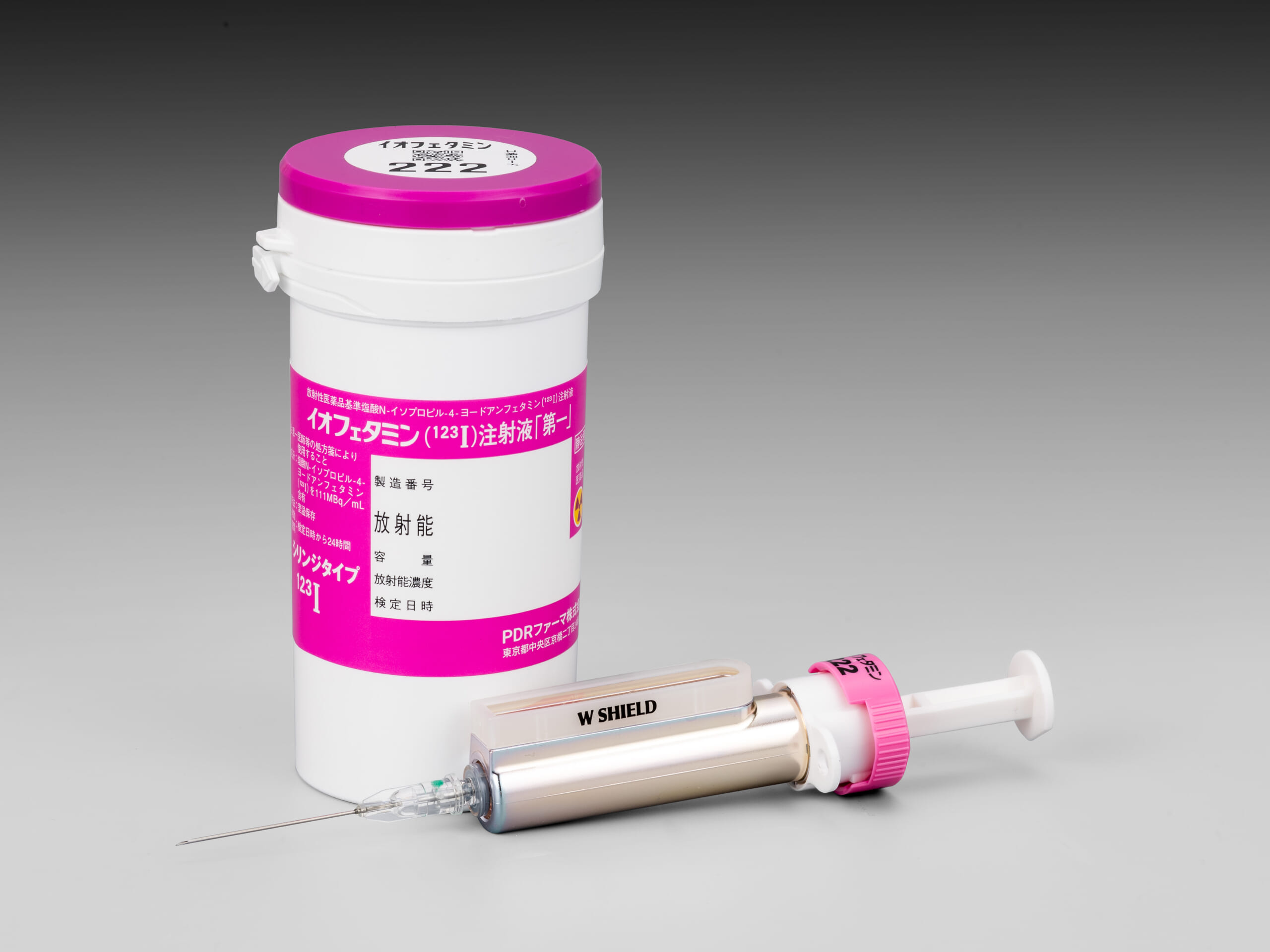 イオフェタミン(123I)注射液「第一」局所脳血流診断薬
イオフェタミン(123I)注射液「第一」局所脳血流診断薬
塩酸 N-イソプロピル-4-ヨードアンフェタミン(123I)注射液 -
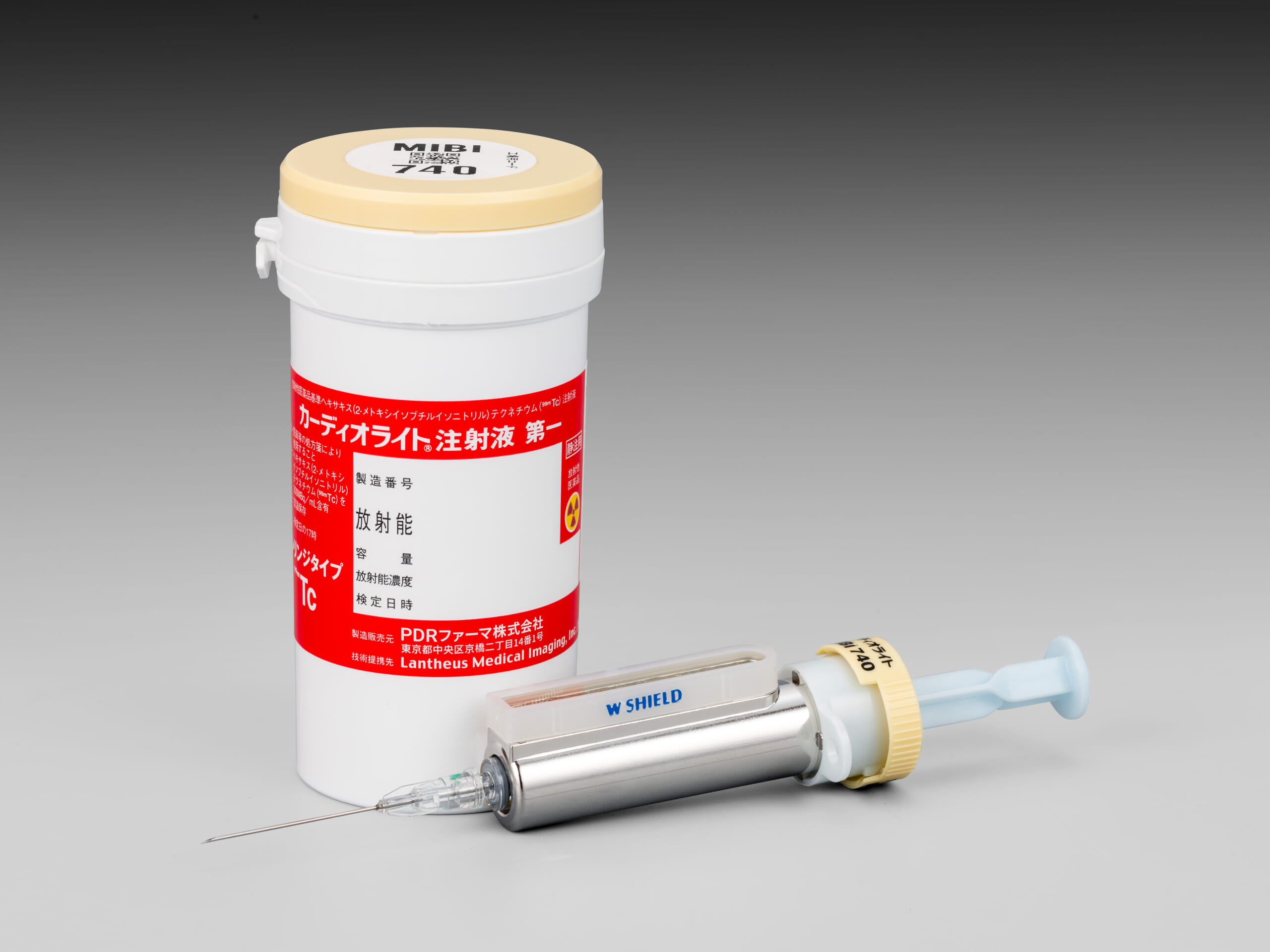 カーディオライト®注射液第一心臓疾患診断薬・心機能診断薬・副甲状腺疾患診断薬
カーディオライト®注射液第一心臓疾患診断薬・心機能診断薬・副甲状腺疾患診断薬
ヘキサキス(2-メトキシイソブチルイソニトリル)テクネチウム(99mTc)注射液
-
 カーディオライト®第一心臓疾患診断薬・心機能診断薬・副甲状腺疾患診断薬
カーディオライト®第一心臓疾患診断薬・心機能診断薬・副甲状腺疾患診断薬
ヘキサキス(2-メトキシイソブチルイソニトリル)テクネチウム(99mTc)注射液 調製用
-
 ウルトラテクネカウ®脳・甲状腺・唾液腺及び異所性胃粘膜疾患診断薬・局所肺換気機能診断薬
ウルトラテクネカウ®脳・甲状腺・唾液腺及び異所性胃粘膜疾患診断薬・局所肺換気機能診断薬
過テクネチウム酸ナトリウム(99mTc)注射液ジェネレータ -
 アドステロール®-I131注射液副腎疾患診断薬
アドステロール®-I131注射液副腎疾患診断薬
ヨウ化メチルノルコレステノール(131I)注射液 -
 テクネ®MDP注射液骨疾患診断薬・脳腫瘍及び脳血管障害診断薬
テクネ®MDP注射液骨疾患診断薬・脳腫瘍及び脳血管障害診断薬
メチレンジホスホン酸テクネチウム(99mTc)注射液 -
 テクネ®MDPキット骨疾患診断薬・脳腫瘍及び脳血管障害診断薬
テクネ®MDPキット骨疾患診断薬・脳腫瘍及び脳血管障害診断薬
メチレンジホスホン酸テクネチウム(99mTc)注射液 調製用 -
 フルデオキシグルコース(18F)静注「FRI」悪性腫瘍診断薬・虚血性心疾患診断薬・てんかん診断薬
フルデオキシグルコース(18F)静注「FRI」悪性腫瘍診断薬・虚血性心疾患診断薬・てんかん診断薬
フルデオキシグルコース(18F)注射液 -
 テクネ®MAG3キット腎及び尿路疾患診断薬
テクネ®MAG3キット腎及び尿路疾患診断薬
メルカプトアセチルグリシルグリシルグリシンテクネチウム(99mTc)注射液 調製用 -
 テクネ®MAG3注射液腎及び尿路疾患診断薬
テクネ®MAG3注射液腎及び尿路疾患診断薬
メルカプトアセチルグリシルグリシルグリシンテクネチウム(99mTc)注射液 -
 オクトレオスキャン®静注用セット神経内分泌腫瘍診断薬
オクトレオスキャン®静注用セット神経内分泌腫瘍診断薬
塩化インジウム(111In )溶液(ペンテトレオチド用)/ペンテトレオチド -
 ミオMIBG®-I123注射液心交感神経診断薬・神経芽腫診断薬・褐色細胞腫診断薬
ミオMIBG®-I123注射液心交感神経診断薬・神経芽腫診断薬・褐色細胞腫診断薬
3-ヨードベンジルグアニジン(123I)注射液 -
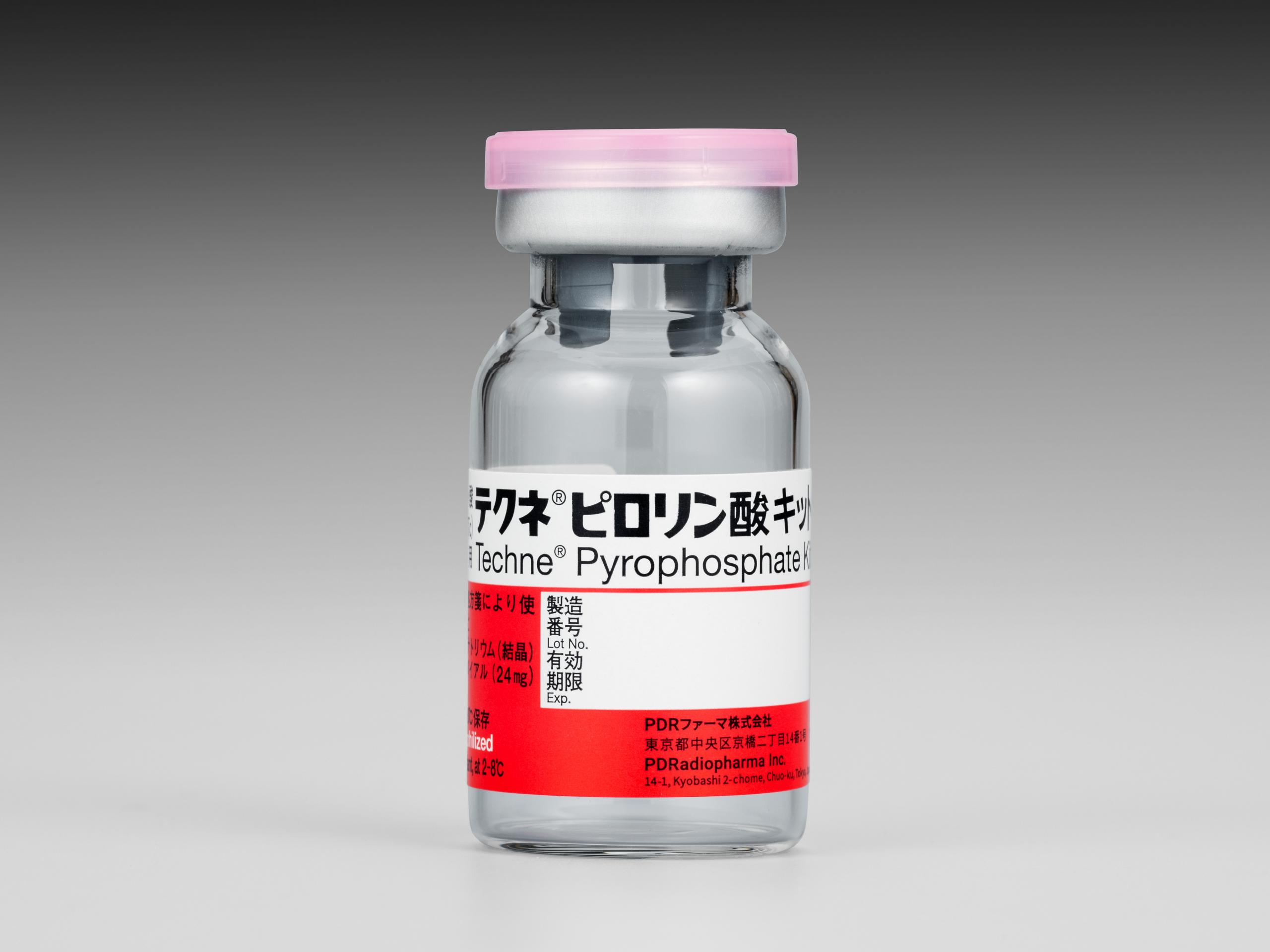 テクネ®ピロリン酸キット心疾患診断薬・骨疾患診断薬
テクネ®ピロリン酸キット心疾患診断薬・骨疾患診断薬
ピロリン酸テクネチウム(99mTc)注射液 調製
-
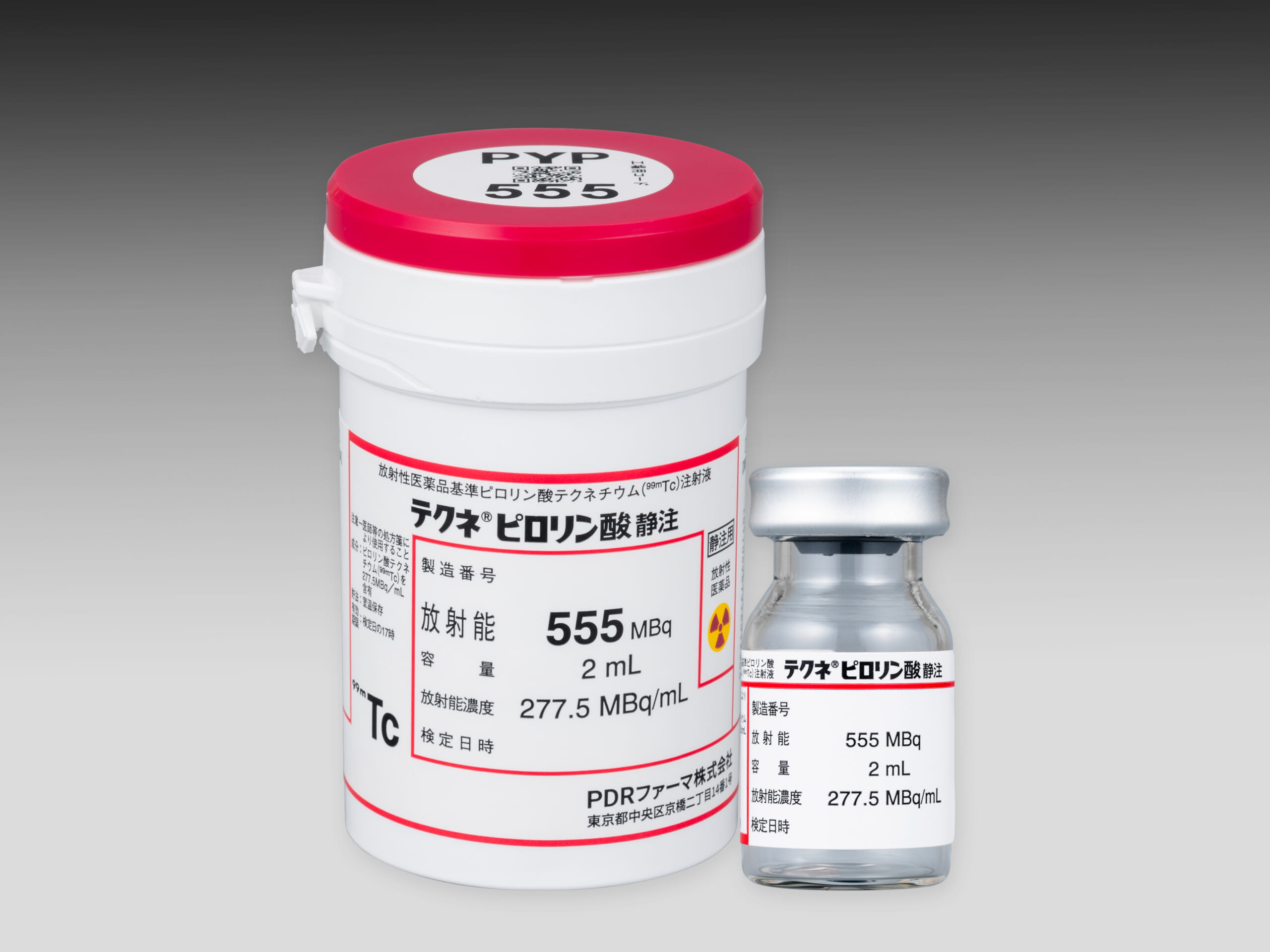 テクネ®ピロリン酸静注骨疾患診断薬
テクネ®ピロリン酸静注骨疾患診断薬
ピロリン酸テクネチウム(99mTc)注射液 -
 アミヴィッド®静注アミロイドイメージング剤
アミヴィッド®静注アミロイドイメージング剤
フロルベタピル(18F)注射液 -
 タウヴィッド®静注タウイメージング剤
タウヴィッド®静注タウイメージング剤
フロルタウシピル(18F)注射液 -
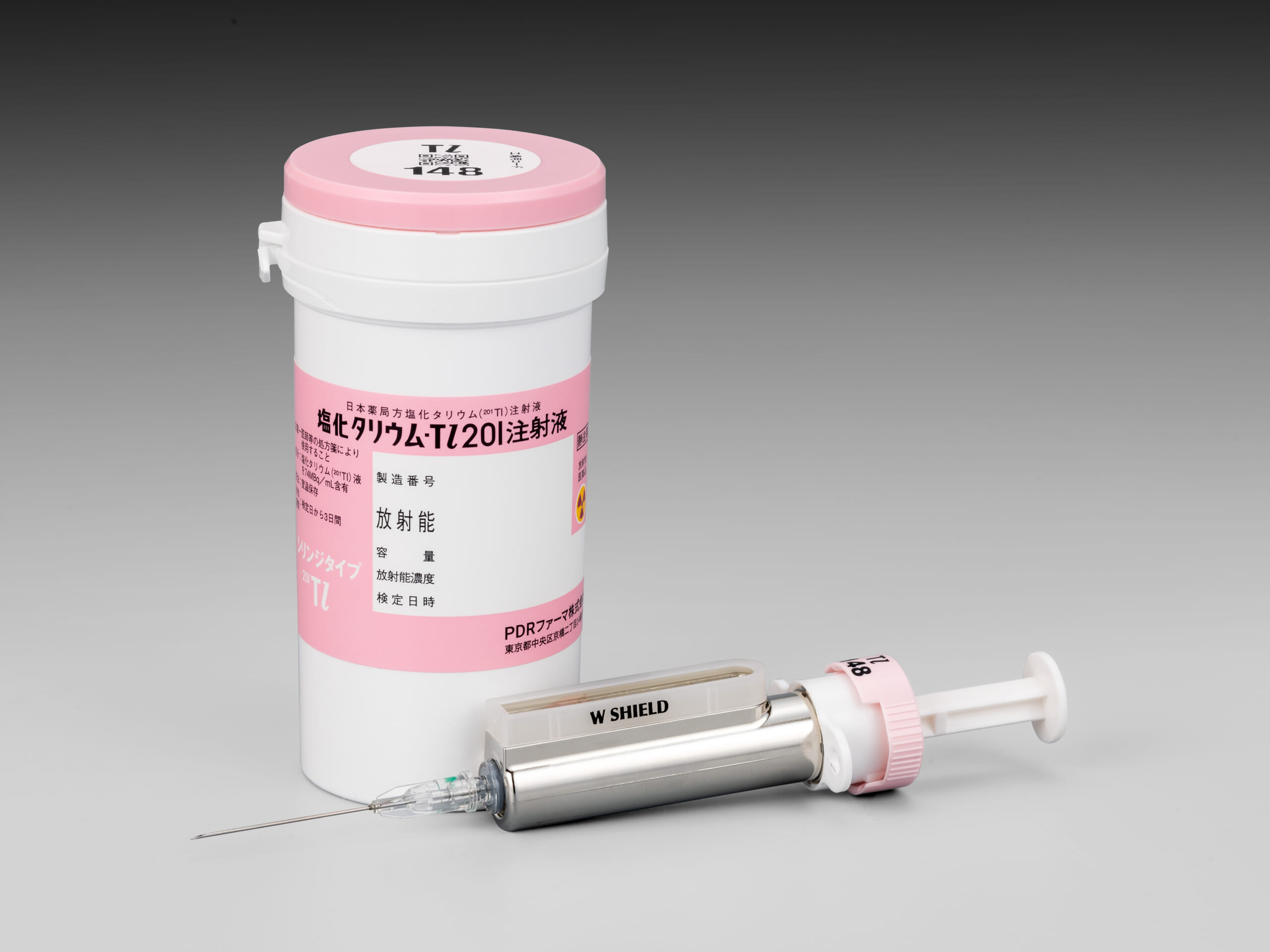 塩化タリウム-Tl201注射液心臓疾患診断薬・腫瘍(脳、甲状腺、肺、骨・軟部、縦隔)診断薬
塩化タリウム-Tl201注射液心臓疾患診断薬・腫瘍(脳、甲状腺、肺、骨・軟部、縦隔)診断薬
副甲状腺疾患診断薬
塩化タリウム(201Tl)注射液 -
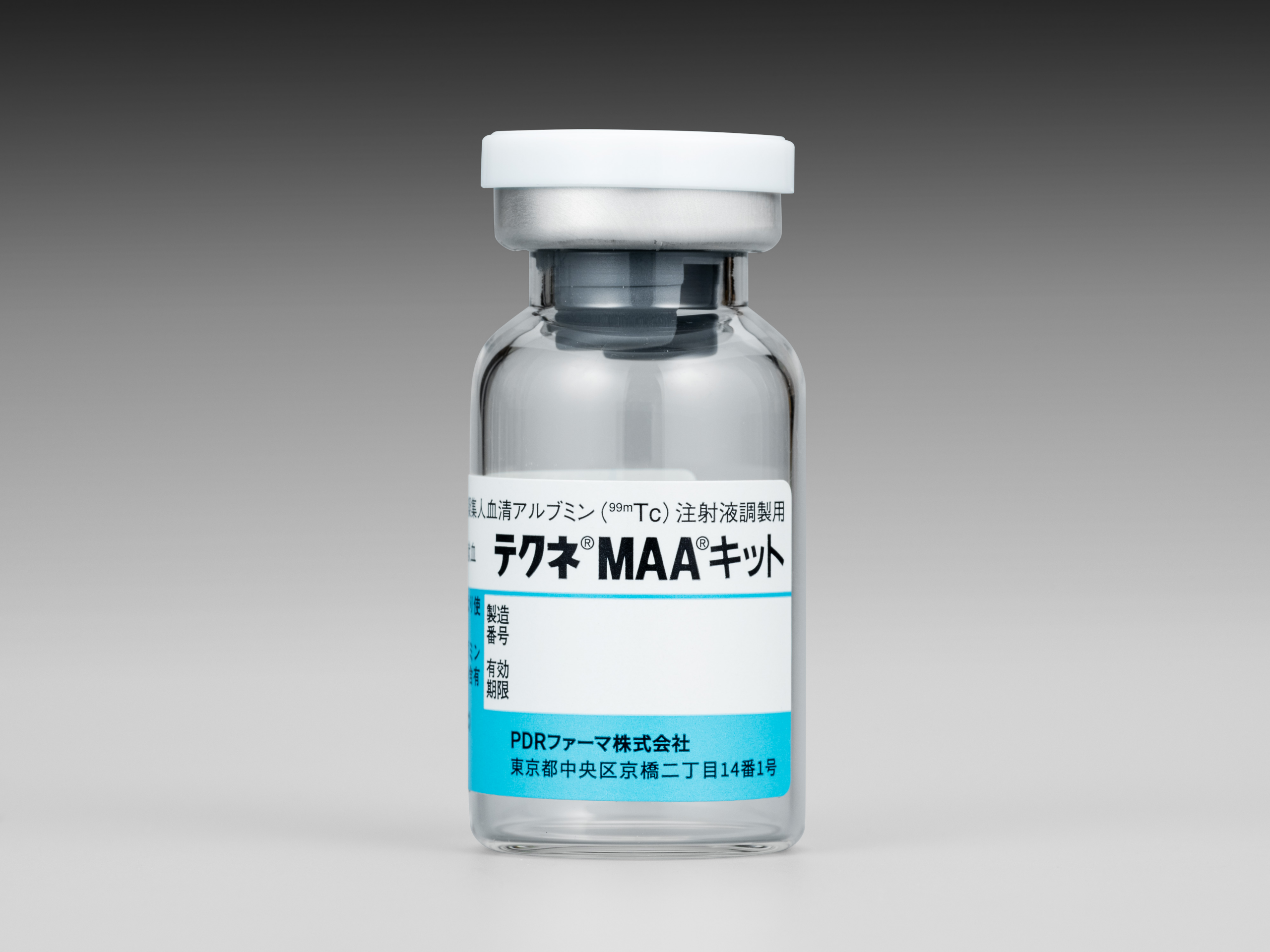 テクネ®MAA®キット肺血流分布異常部位診断薬
テクネ®MAA®キット肺血流分布異常部位診断薬
テクネチウム大凝集人血清アルブミン(99mTc)注射液 調製用 -
 テクネ®DTPAキット腎疾患診断薬
テクネ®DTPAキット腎疾患診断薬
ジエチレントリアミン五酢酸テクネチウム(99mTc)注射液 調製用 -
 テクネ®DMSAキット腎疾患診断薬
テクネ®DMSAキット腎疾患診断薬
ジメルカプトコハク酸テクネチウム(99mTc)注射液 調製用 -
 テクネ®フチン酸キット肝脾疾患診断薬・センチネルリンパ節同定用薬
テクネ®フチン酸キット肝脾疾患診断薬・センチネルリンパ節同定用薬
フィチン酸テクネチウム(99mTc)注射液 調製用
